私たちが日常的に使う塩、つまり塩化ナトリウム。この物質の溶解度が変わらない理由について考えたことはありますか?塩化ナトリウムの溶解度は、温度や圧力に対して非常に安定しているため、私たちの生活において重要な役割を果たしています。この特性は、料理や食品保存だけでなく、化学実験や産業プロセスでも欠かせません。
塩化ナトリウムとは
塩化ナトリウムは、化学式NaClを持つ無機化合物です。食塩とも呼ばれ、広く利用されています。以下に塩化ナトリウムに関する重要なポイントを挙げます。
- 用途が多岐にわたる:塩化ナトリウムは、食品の保存や味付け、産業用途、医療分野で使われます。
- 溶解性が特徴的:塩化ナトリウムは水に溶けやすく、温度が上昇しても溶解度が大きく変わりません。
- 結晶構造を持つ:塩化ナトリウムは立方体の結晶を形成し、可視的にも特長があります。
- 安全性が高い:食用の塩化ナトリウムは、適切に使用すれば健康に害を及ぼさないとされています。
- 電解質としての役割:体内で電解質として機能し、生理的なバランスを維持します。
溶解度の基本
塩化ナトリウムの溶解度を理解するためには、基本的な定義とその性質を知ることが重要です。ここでは、溶解度の意義とそれに影響を与える要因について詳しく説明します。
溶解度の定義
溶解度とは、特定の温度で一定量の溶媒に溶ける溶質の最大量を指します。塩化ナトリウムの場合、水に溶けやすく、一定の条件下では溶解度が変わらない特性があります。以下は、塩化ナトリウムの溶解度に関連するポイントです。
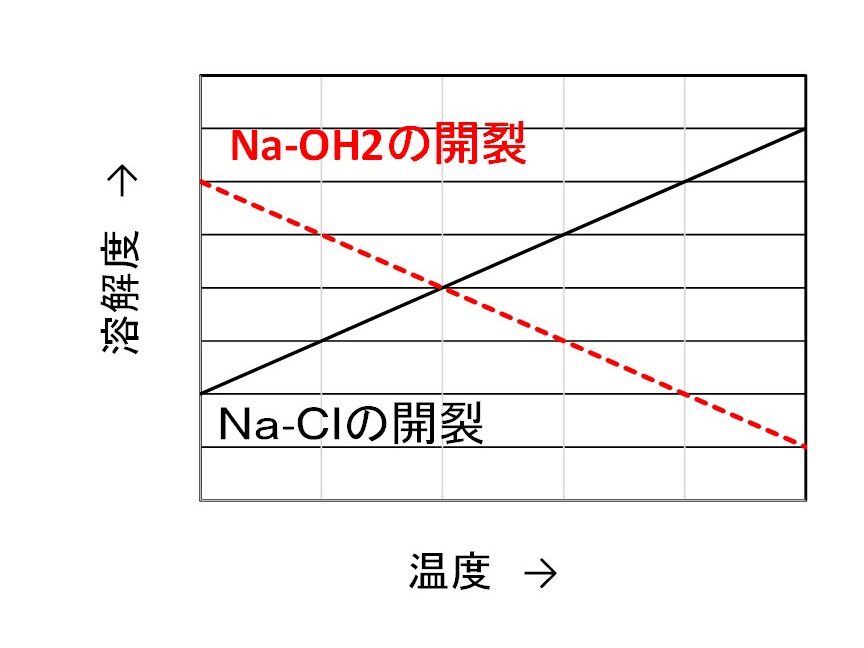
- 温度: 一般的に、温度が上昇すると多くの物質の溶解度が増加しますが、塩化ナトリウムはこの原則から外れるとされています。
- 圧力: ガスの溶解度は圧力に依存しますが、塩化ナトリウムのような固体の溶解度は圧力の影響を受けにくいです。
- 溶媒の性質: 水の性質が塩化ナトリウムの溶解に大きく関わります。水は極性溶媒であるため、塩化ナトリウムが容易に溶解します。
影響を与える要因
塩化ナトリウムの溶解度に影響を与える要因は多岐にわたります。具体的な要因を以下に示します。
- 粒子の大きさ: 粒子が小さいほど、表面積が増え、溶解が促進されます。
- 混合の程度: 溶質と溶媒が均一に混ざることで、溶解が進みやすくなります。
- イオン強度: 溶液中の他のイオンの存在が溶解度に影響を与えることがあります。
塩化ナトリウムの溶解度
塩化ナトリウムの溶解度は、温度や圧力に対して非常に安定していることが特長です。このセクションでは、塩化ナトリウムの水中での挙動と温度との関係について詳しく説明します。
水中での挙動
塩化ナトリウム(NaCl)は、水に溶けるとイオンに解離します。次の点を考慮してください。
- 水分子の作用: 水分子が塩化ナトリウムの結晶を囲み、イオンを引き離します。
- イオンの移動: Na+ および Cl– イオンが水中に広がり、均一な溶液を形成します。
- 濃度の変化: 溶液中のイオン濃度が高まると、さらなる溶解が難しくなる場合があります。
このように、塩化ナトリウムは水に溶けてイオンを生成し、独特な性質を持つ溶液を作ります。
温度との関係
塩化ナトリウムの溶解度は温度に対してあまり変わりません。以下の点を確認しましょう。
- 常温での安定性: 常温(水温約20℃)では、塩化ナトリウムの溶解度は約36g/100mLです。
- 高温時の変化: 温度が上がっても、溶解度がわずかに増加するだけです。
- 結晶構造の影響: 塩化ナトリウムの結晶構造が、溶解度の変化を抑える要因となります。
溶解度が変わらない理由
塩化ナトリウムの溶解度が変わらない理由は、主に化学的要因と環境要因に起因しています。これらの要素がどのように影響を及ぼすのか、以下に詳しく説明します。
化学的要因
- イオン電荷のバランス: 塩化ナトリウムはNa⁺とCl⁻という二つのイオンから成り立っています。このイオンは水中で安定して存在し、お互いに引き合う力が強いです。
- 結晶構造: 塩化ナトリウムは立方体の結晶構造を持っています。この構造が溶解時にイオンが安定して分散するのを助けます。
- 溶解エンタルピー: 溶解時に必要なエネルギーが小さいため、塩化ナトリウムの溶解度は高いまま保たれます。
環境要因
- 温度の影響: 通常、温度が上昇すると一般的に溶解度も増加しますが、塩化ナトリウムに関しては、温度の変化がその溶解度に与える影響は限られています。
- 圧力の影響: 塩化ナトリウムの溶解度は圧力の変化に対して非常に安定しています。具体的には、圧力が変わってもその溶解度はほぼ変化しません。
- 水の性質: 水分子は極性を持つため、Na⁺とCl⁻イオンとの相互作用が強く、塩化ナトリウムが水に溶けやすくなります。
溶解度の実用的意味
塩化ナトリウムの溶解度が安定していることは、様々な分野で重要な意味を持ちます。この特性が工業や日常生活にどのように影響を与えるのか、具体的に見ていきましょう。
工業への影響
- 常温状態での溶解度が一定で、製品の品質を安定化させる。
- 塩化ナトリウムは、製造過程でその溶解度が変わらないため、製品の一貫性を保つ。
- 温度変化に強く、工業的プロセスでの信頼性を向上させる。
- 工業用の化学反応において、高温や低温条件下でも溶解度が変化しないため、効率的な生産が可能。
- 輸送コストの削減が見込まれる。
- 溶解度が安定しているため、一度調合された塩水の品質が保持されることで、再処理の必要が減少。
日常生活での応用
- 食品の保存における役割。
- 塩化ナトリウムは、食材の保護や保存に関与し、腐敗を防ぐ効果がある。
- 日常的な調味料としての利用。
- 我々が料理をする際、塩化ナトリウムの安定した溶解度が、風味の一貫性を確保。
- 医療分野での重要性。
- 生理食塩水など、塩化ナトリウムを含む液体が点滴や補液として使われ、体液のバランスを維持。
結論
塩化ナトリウムの溶解度が変わらない理由は、化学的要因と環境要因の相互作用にあります。この安定性は、料理や食品保存、工業プロセスにおいて重要な役割を果たしています。温度や圧力の変化に強く、一定の条件下での利用が可能なため、私たちの生活に欠かせない存在です。
また、塩化ナトリウムの結晶構造がその特性を支え、様々な分野での応用を可能にしています。これにより、私たちは安心してこの物質を日常生活や産業で活用できるのです。